식품의약품안전처는 7일 금연치료보조제 '바레니클린' 성분 함유 의약품 중 니트로사민 계열 불순물[N-nitroso-varenicline(엔-니트로소-바레니클린), NNV]에 대한 안전성 조사 결과 인체 위해 우려는 매우 낮은 수준이라고 밝혔다.
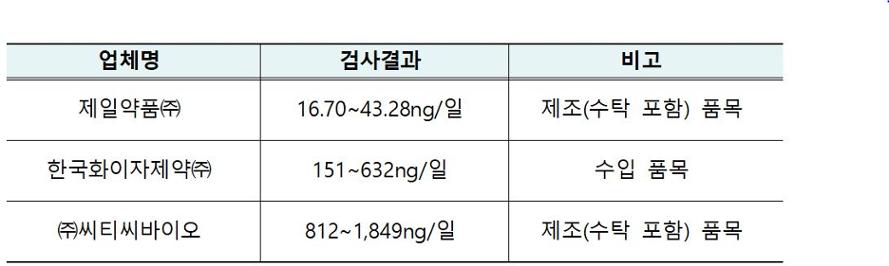
식약처에 따르면 국내 바레니클린 의약품에서 NNV가 16.70~1849ng/일으로 낮은 수준으로 검출됐으며, 인체영향 평가 결과 건강 영향 우려는 경미한 것으로 나타났다.
다만 NNV가 국내 유통 중인 모든 제품에서 검출됨에 따라 ▲복용 환자에 대한 영향 평가 ▲NNV 1일 섭취 허용량 설정·검출량별 조치 기준 ▲전문가와 환자 안내 사항 등 단계적인 안전관리 대책을 마련해 시행 중이다.
바레니클린 의약품을 복용한 환자의 인체영향 평가는 ▲국내 유통 중 제품의 일일 최대복용량 ▲NNV 검사 결과 ▲국민건강보험공단의 금연치료지원사업에 참여한 환자의 실제 투약 일수 등을 종합적으로 고려해 의약품 분야 국제 가이드라인에 따라 수행했다.
인체영향평가 결과 NNV 검출량은 추가로 암이 발생할 가능성이 10만명 중 0.194~0.391명인 것으로 나타났다. 의약품 분야 국제 가이드라인에 따르면 10만명 중 1명 이하인 경우는 ‘무시할 수 있는 수준’에 해당된다.
식약처는 중앙약사심의위원회 자문을 받아 화학구조가 매우 유사한 니트로사민 계열 물질인 NTHP(N-Nitroso-1,2,3,6-tetrahydropyridine)의 독성 값 등을 참고해 NNV의 1일 섭취 허용량을 37ng/일(미국 등 해외 규제기관과 동일 수준)로 설정했다.
식약처는 "‘한시적 출하허용기준’을 185ng/일로 설정했다"면서 "시중 출하 예정인 바레니클린 의약품에 대해서는 185ng/일 이하인 제품만을 출하하도록 조치할 예정"이라고 밝혔다.
이 같은 결정은 ▲바레니클린 의약품 중 NNV 인체영향평가 결과 위해 우려가 거의 없는 점 ▲NNV 검출량을 이번에 설정한 1일 섭취 허용량(37ng/일) 이하로 단번에 저감화하기 어려운 점 ▲미국에서 한시적 출하허용기준을 185ng/일로 설정한 점 ▲금연치료보조제의 환자 접근성 ▲중앙약심 자문 결과 등을 종합적으로 검토한 결과다.
한편 이미 시중에 유통 중인 바레니클린 의약품 중에서 NNV 검출량이 733ng/일을 초과한 모든 제품은 업체에서 자발적으로 회수하기로 했다.
회수의약품은 씨티씨바이오에서 제조한 비보존제약 제로코틴정0.5mg, 1mg, 씨티씨바이오 니코브렉정0.5mg, 1mg, 한미약품 노코틴에스정0.5밀리그램, 1밀리그램 등이다.
이 같은 결정은 ▲바레니클린 의약품 중 NNV 인체영향평가 결과 위해 우려가 거의 없는 점 ▲금연치료보조제의 공급 차질이 우려되는 점 ▲NNV 검출이 전 세계적인 상황속에서 미국 등 주요 국가가 유통 중인 제품에 대해 733ng/일 이내로 검출된 제품(제조번호)은 회수 등 조치 없이 유통을 허용하고 있는 점 ▲중앙약심 자문 결과 등에 따른 조치다.
식약처는 "NNV 검출량을 1일 섭취 허용량 이하로 최대한 신속하게 저감화할 수 있도록 관련 업계와 지속적으로 의사소통하며 협력체계를 유지하고 있다"면서 "저감화가 완료되면 그 결과를 추가 발표하겠다"고 밝혔다.
이어 "이미 해당 제품(제조번호)을 처방받은 환자분들은 의약품 복용을 임의로 중단하지 말고, 계속 복용하거나 대체 의약품으로 전환 필요성 등은 반드시 의사·약사와 상담해야 한다"고 권고했다.
만약 상담 결과 대체 의약품으로 전환이 필요한 경우 건보공단의 금연치료지원사업 참여의료기관(2021년기준, 1만 5085개소)에서 금연치료보조제 처방을 받은 후 약국에서 조제가 가능하다고 안내했다.
식약처는 "바레니클린 의약품에 대한 각국 규제기관의 규제 동향, 산업계의 불순물 저감화 진행 상황, 의약품 공급 상황 등을 면밀히 검토해 필요시 한시적 출하허용기준 등을 수정·보완할 예정이며 주요 변경사항을 보건전문가와 국민들에게 적극 알리겠다"면서 "앞으로도 국민에게 안전하고 효과적인 고품질의 의약품을 제공하기 위해 규제과학에 기반해 의약품 안전관리 제도를 지속적으로 개선하고 제약 업체들과도 적극적으로 협력하겠다"고 강조했다.
식약처에 따르면 국내 바레니클린 의약품에서 NNV가 16.70~1849ng/일으로 낮은 수준으로 검출됐으며, 인체영향 평가 결과 건강 영향 우려는 경미한 것으로 나타났다.
다만 NNV가 국내 유통 중인 모든 제품에서 검출됨에 따라 ▲복용 환자에 대한 영향 평가 ▲NNV 1일 섭취 허용량 설정·검출량별 조치 기준 ▲전문가와 환자 안내 사항 등 단계적인 안전관리 대책을 마련해 시행 중이다.
바레니클린 의약품을 복용한 환자의 인체영향 평가는 ▲국내 유통 중 제품의 일일 최대복용량 ▲NNV 검사 결과 ▲국민건강보험공단의 금연치료지원사업에 참여한 환자의 실제 투약 일수 등을 종합적으로 고려해 의약품 분야 국제 가이드라인에 따라 수행했다.
인체영향평가 결과 NNV 검출량은 추가로 암이 발생할 가능성이 10만명 중 0.194~0.391명인 것으로 나타났다. 의약품 분야 국제 가이드라인에 따르면 10만명 중 1명 이하인 경우는 ‘무시할 수 있는 수준’에 해당된다.
식약처는 중앙약사심의위원회 자문을 받아 화학구조가 매우 유사한 니트로사민 계열 물질인 NTHP(N-Nitroso-1,2,3,6-tetrahydropyridine)의 독성 값 등을 참고해 NNV의 1일 섭취 허용량을 37ng/일(미국 등 해외 규제기관과 동일 수준)로 설정했다.
식약처는 "‘한시적 출하허용기준’을 185ng/일로 설정했다"면서 "시중 출하 예정인 바레니클린 의약품에 대해서는 185ng/일 이하인 제품만을 출하하도록 조치할 예정"이라고 밝혔다.
이 같은 결정은 ▲바레니클린 의약품 중 NNV 인체영향평가 결과 위해 우려가 거의 없는 점 ▲NNV 검출량을 이번에 설정한 1일 섭취 허용량(37ng/일) 이하로 단번에 저감화하기 어려운 점 ▲미국에서 한시적 출하허용기준을 185ng/일로 설정한 점 ▲금연치료보조제의 환자 접근성 ▲중앙약심 자문 결과 등을 종합적으로 검토한 결과다.
한편 이미 시중에 유통 중인 바레니클린 의약품 중에서 NNV 검출량이 733ng/일을 초과한 모든 제품은 업체에서 자발적으로 회수하기로 했다.
회수의약품은 씨티씨바이오에서 제조한 비보존제약 제로코틴정0.5mg, 1mg, 씨티씨바이오 니코브렉정0.5mg, 1mg, 한미약품 노코틴에스정0.5밀리그램, 1밀리그램 등이다.
이 같은 결정은 ▲바레니클린 의약품 중 NNV 인체영향평가 결과 위해 우려가 거의 없는 점 ▲금연치료보조제의 공급 차질이 우려되는 점 ▲NNV 검출이 전 세계적인 상황속에서 미국 등 주요 국가가 유통 중인 제품에 대해 733ng/일 이내로 검출된 제품(제조번호)은 회수 등 조치 없이 유통을 허용하고 있는 점 ▲중앙약심 자문 결과 등에 따른 조치다.
식약처는 "NNV 검출량을 1일 섭취 허용량 이하로 최대한 신속하게 저감화할 수 있도록 관련 업계와 지속적으로 의사소통하며 협력체계를 유지하고 있다"면서 "저감화가 완료되면 그 결과를 추가 발표하겠다"고 밝혔다.
이어 "이미 해당 제품(제조번호)을 처방받은 환자분들은 의약품 복용을 임의로 중단하지 말고, 계속 복용하거나 대체 의약품으로 전환 필요성 등은 반드시 의사·약사와 상담해야 한다"고 권고했다.
만약 상담 결과 대체 의약품으로 전환이 필요한 경우 건보공단의 금연치료지원사업 참여의료기관(2021년기준, 1만 5085개소)에서 금연치료보조제 처방을 받은 후 약국에서 조제가 가능하다고 안내했다.
식약처는 "바레니클린 의약품에 대한 각국 규제기관의 규제 동향, 산업계의 불순물 저감화 진행 상황, 의약품 공급 상황 등을 면밀히 검토해 필요시 한시적 출하허용기준 등을 수정·보완할 예정이며 주요 변경사항을 보건전문가와 국민들에게 적극 알리겠다"면서 "앞으로도 국민에게 안전하고 효과적인 고품질의 의약품을 제공하기 위해 규제과학에 기반해 의약품 안전관리 제도를 지속적으로 개선하고 제약 업체들과도 적극적으로 협력하겠다"고 강조했다.


