[메디게이트뉴스 서민지 기자] 새로운 경구용 항응고제(NOAC·Non-Vitamin K Antagonist Oral Anticoagulant)의 재심사 기간(PMS)이 만료 또는 만료 예정인 가운데, 잇따라 국내제약사들이 제네릭 출시를 위한 임상시험을 추진하고 있다.
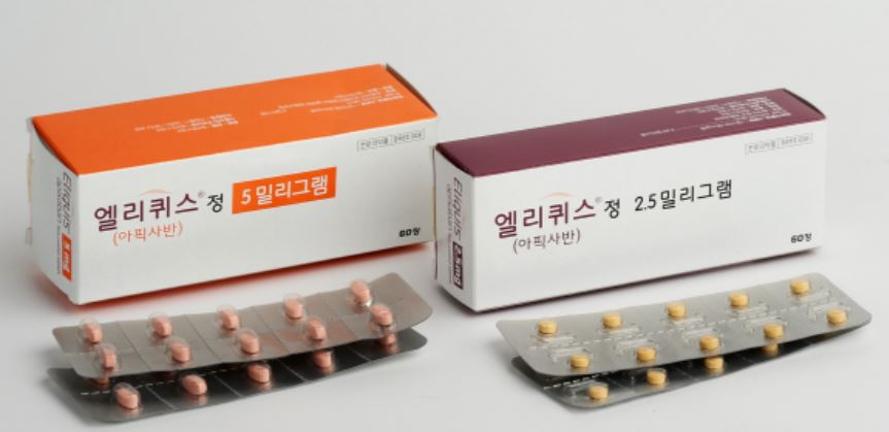 앞서 지난 13일 하나제약은 식품의약품안전처로부터 원픽사반정5밀리그램(성분명 아픽사반·Apixaban 5mg)과 대조약인 한국BMS제약 엘리퀴스정 5밀리그램(아픽사반)의 생물학적 동등성 평가를 위한 임상시험을 허가받았다.
앞서 지난 13일 하나제약은 식품의약품안전처로부터 원픽사반정5밀리그램(성분명 아픽사반·Apixaban 5mg)과 대조약인 한국BMS제약 엘리퀴스정 5밀리그램(아픽사반)의 생물학적 동등성 평가를 위한 임상시험을 허가받았다.
유영제약 역시 지난 7월 유픽스정5밀리그램(아픽사반)과 엘리퀴스정5밀리그램(아픽사반)의 생물학적 동등성평가를 위한 임상시험을 허가받았다.
이들 임상의 대상질환명(적응증)은 고관절 또는 슬관절 치환술을 받은 성인 환자에서 정맥혈전색전증의 예방, 비판막성 심방세동 환자에서 뇌졸중 및 전신 색전증의 위험 감소 심재성 정맥혈전증 및 폐색전증의 치료 심재성 정맥혈전증 및 폐색전증의 재발 위험 감소 등이며, 임상실시기관도 모두 에이치플러스양지병원이다.
1차 유효성 평가변수는 에픽사반의 혈장농도-시간 곡선하 면적(AUCt), 최대 혈청 농도(Cmax)다.
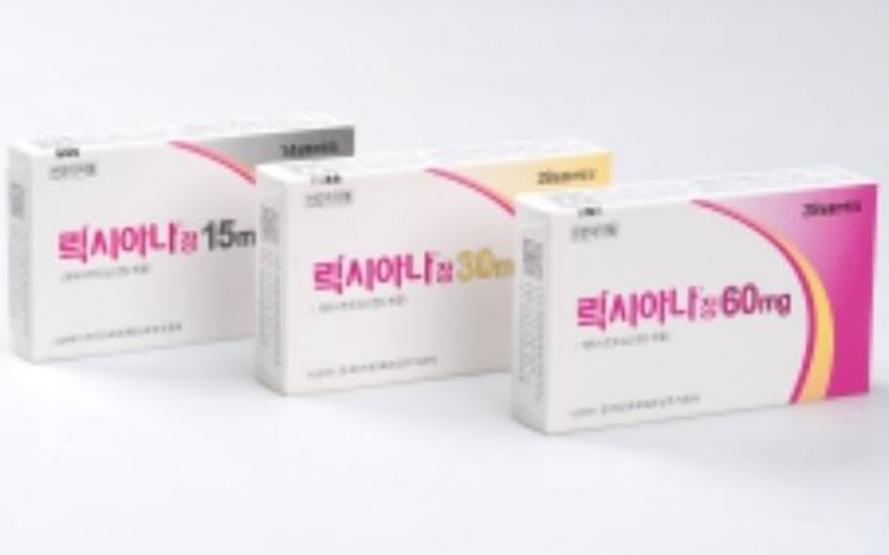 또한 이달 초 동아에스티(동아ST)도 DA-5209정 60밀리그램(성분명 에독사반토실산염수화물)과 한국다이이찌산쿄 릭시아나정 60밀리그램의 생동성 평가 임상을 승인받았다.
또한 이달 초 동아에스티(동아ST)도 DA-5209정 60밀리그램(성분명 에독사반토실산염수화물)과 한국다이이찌산쿄 릭시아나정 60밀리그램의 생동성 평가 임상을 승인받았다.
시험실시기관은 에이치플러스양지병원이며, 목표대상자수는 60명, 기간은 오는 11월부터 2021년 7월까지다.
해당 임상의 1차 유효성 평가변수는 에독사반의 혈장농도-시간 곡선하 면적(AUCt), 최대 혈청 농도(Cmax)다. 대상질환은 심혈관질환(Cardiovascular)으로, 적응증은 ▲비판막성 심방세동 환자에서 뇌졸중 및 전신색전증의 위험 감소 ▲심재성 정맥혈전증 및 폐색전증의 치료 ▲심재성 정맥혈전증 및 폐색전증의 재발 위험 감소 등이다.
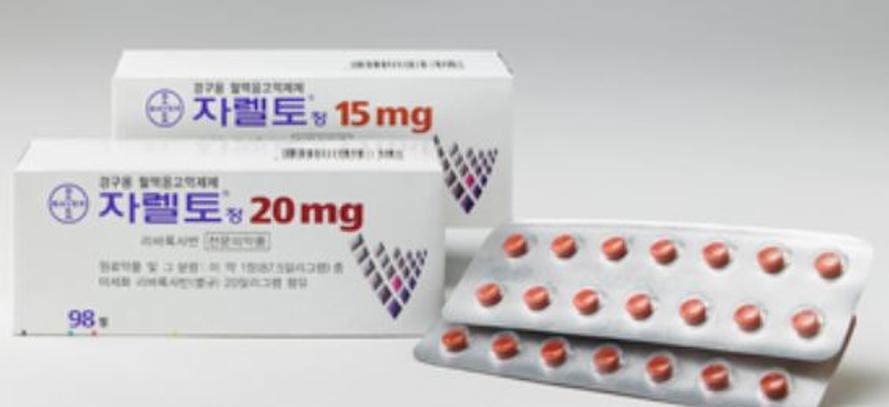 GC녹십자도 NOAC 제네릭 출시를 위한 생동성 임상을 추진 중이다. 지난달 녹십자는 식약처로부터 GC7002 20mg과 바이엘코리아 자렐토정20밀리그램(리바록사반)의 생동성 평가 시행계획서를 허가받고 임상에 돌입했다. 임상시험 기간은 지난달부터 오는 2021년 12월까지다.
GC녹십자도 NOAC 제네릭 출시를 위한 생동성 임상을 추진 중이다. 지난달 녹십자는 식약처로부터 GC7002 20mg과 바이엘코리아 자렐토정20밀리그램(리바록사반)의 생동성 평가 시행계획서를 허가받고 임상에 돌입했다. 임상시험 기간은 지난달부터 오는 2021년 12월까지다.
적응증은 ▲비판막성 심방세동 환자에서 뇌졸중 및 전신 색전증의 위험 감소 ▲심재성 정맥혈전증 및 폐색전증의 치료 ▲심재성 정맥혈전증 및 폐색전증의 재발 위험 감소 ▲하지의 주요 정형외과 수술(슬관절 또는 고관절 치환술)을 받은 성인 환자의 정맥혈전색전증 예방 등이며, 목표 시험 대상자 수는 30명이다. 임상의 1차 유효성 평가변수는 리바록사반의 AUCt 및 Cmax다.
일동제약과 유영제약도 지난 8월 각각 제네릭 출시를 위한 자렐토정과의 생동성 시험을 허가받았으며, 콜마파마 역시 지난 5월 생동성 시험을 허가 받고 임상을 진행 중이다.
한편 올해로 접어들면서 NOAC 시장의 성장세가 둔화되고 있으며 동시에 내년부터 이어질 제네릭 출시 러쉬까지 가세하면 오리지널의 시장 입지는 더욱 좁아질 것으로 전망된다.
실제 유비스트에 따르면 가장 최근 개발된 다이이찌산쿄 릭시아나의 올해 상반기 처방조제액은 317억 3095만원으로 지난해 상반기(287억 982만원) 보다 10.52% 증가했으나, BMS의 엘리퀴스 올해 상반기 처방액은 244억 1184만원으로 전년 상반기 대비 1.76% 증가하는 데 그쳤다.
특히 잇따라 제네릭 출시가 예고되고 있는 자렐토의 경우 올해 상반기 처방액은 247억 8717만원으로 지난해 상반기 처방액보다 0.88% 감소했다.
유영제약 역시 지난 7월 유픽스정5밀리그램(아픽사반)과 엘리퀴스정5밀리그램(아픽사반)의 생물학적 동등성평가를 위한 임상시험을 허가받았다.
이들 임상의 대상질환명(적응증)은 고관절 또는 슬관절 치환술을 받은 성인 환자에서 정맥혈전색전증의 예방, 비판막성 심방세동 환자에서 뇌졸중 및 전신 색전증의 위험 감소 심재성 정맥혈전증 및 폐색전증의 치료 심재성 정맥혈전증 및 폐색전증의 재발 위험 감소 등이며, 임상실시기관도 모두 에이치플러스양지병원이다.
1차 유효성 평가변수는 에픽사반의 혈장농도-시간 곡선하 면적(AUCt), 최대 혈청 농도(Cmax)다.
시험실시기관은 에이치플러스양지병원이며, 목표대상자수는 60명, 기간은 오는 11월부터 2021년 7월까지다.
해당 임상의 1차 유효성 평가변수는 에독사반의 혈장농도-시간 곡선하 면적(AUCt), 최대 혈청 농도(Cmax)다. 대상질환은 심혈관질환(Cardiovascular)으로, 적응증은 ▲비판막성 심방세동 환자에서 뇌졸중 및 전신색전증의 위험 감소 ▲심재성 정맥혈전증 및 폐색전증의 치료 ▲심재성 정맥혈전증 및 폐색전증의 재발 위험 감소 등이다.
적응증은 ▲비판막성 심방세동 환자에서 뇌졸중 및 전신 색전증의 위험 감소 ▲심재성 정맥혈전증 및 폐색전증의 치료 ▲심재성 정맥혈전증 및 폐색전증의 재발 위험 감소 ▲하지의 주요 정형외과 수술(슬관절 또는 고관절 치환술)을 받은 성인 환자의 정맥혈전색전증 예방 등이며, 목표 시험 대상자 수는 30명이다. 임상의 1차 유효성 평가변수는 리바록사반의 AUCt 및 Cmax다.
일동제약과 유영제약도 지난 8월 각각 제네릭 출시를 위한 자렐토정과의 생동성 시험을 허가받았으며, 콜마파마 역시 지난 5월 생동성 시험을 허가 받고 임상을 진행 중이다.
한편 올해로 접어들면서 NOAC 시장의 성장세가 둔화되고 있으며 동시에 내년부터 이어질 제네릭 출시 러쉬까지 가세하면 오리지널의 시장 입지는 더욱 좁아질 것으로 전망된다.
실제 유비스트에 따르면 가장 최근 개발된 다이이찌산쿄 릭시아나의 올해 상반기 처방조제액은 317억 3095만원으로 지난해 상반기(287억 982만원) 보다 10.52% 증가했으나, BMS의 엘리퀴스 올해 상반기 처방액은 244억 1184만원으로 전년 상반기 대비 1.76% 증가하는 데 그쳤다.
특히 잇따라 제네릭 출시가 예고되고 있는 자렐토의 경우 올해 상반기 처방액은 247억 8717만원으로 지난해 상반기 처방액보다 0.88% 감소했다.


